
Blog
بایومارکر
بیومارکر چیست؟
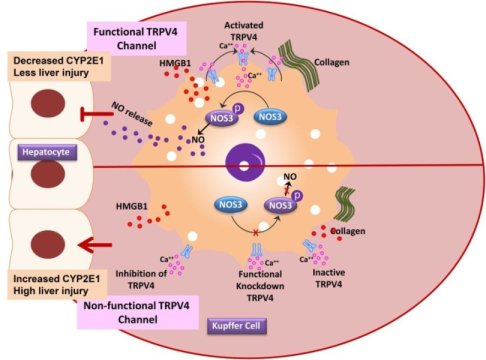
بیومارکرها مولکولهایی هستند که فرایند طبیعی یا غیرطبیعی را در بدن شما نشان میدهند و ممکن است نشانهای از وضعیت یا بیماری باشند. انواع مختلف مولکولها، مانند DNA، ژنها، پروتئینها و هورمونها میتوانند به عنوان نشانگرهای زیستی عمل کنند، زیرا همه آنها در مورد سلامتی اطلاعات بسیاری را در اختیار قرار میدهند. بیومارکرها ممکن است توسط خود بافت سرطانی و یا توسط سلولهای دیگر در بدن در پاسخ به سرطان تولید شوند. آنها میتوانند در خون، مدفوع، ادرار، بافت تومور یا سایر بافتها و یا مایعات بدن یافت شوند. به طور مشخص، نشانگرهای زیستی محدود به سرطان نیستند. بیومارکرها برای بیماریهای قلبی، مولتیپل اسکلروز و بسیاری از بیماریهای دیگر وجود دارد.
یادگیری برخی از حقایق اولیه برای درک اهمیت بیومارکرها در سرطان، داشتن اطلاعات در مورد DNA، RNA و پروتئین مفید است. DNA یک مولکول درون سلولی است که اطلاعات ژنتیکی را حمل میکند و از یک نسل به نسل بعد منتقل میشود RNA یا اسیدریبونوکلئیک شامل اطلاعاتی است که از DNA کپی شده است. سلولهای بدن چندین مولکول RNA مختلف را تشکیل میدهند که برای سنتز مولکولهای پروتئین ضروری هستند. به عنوان مثال، mRNA، یا مولکول های RNA messenger، به عنوان الگوهایی برای تولید پروتئین از واحدهای آمینو اسید عمل میکنند، در حالی که tRNA یا مولکولهای RNA ناقل، واحدهای اسیدآمینه را به ریبوزوم میرسانند. داخل ریبوزوم، فرآیند ترجمه به پروتئین انجام میگیرد.
پروتئین به عملکرد بدن کمک میکند و اساس ساختار بدن مانند پوست و مو است. آنها طیف گستردهای از توابع در داخل بدن انسان دارند. برخی از پروتئینها (آنزیمها) سرعت واکنشهای شیمیایی را افزایش میدهند، برخی (سیتوکنینها) بر عملکرد سیستم ایمنی بدن تاثیر میگذارند و در عین حال سایر پروتئینها که آنتیبادی نامیده میشوند، واکنشهای ایمنی خاص را در پاسخ به آنتیژنها انجام میدهند.
بیومارکرهای سرطانی میتوانند شامل موارد زیر باشند:
• پروتئینها
• جهشهای ژنی (تغییرات)
• بازسازی ژن
• کپیهای اضافی از ژنها
• حذف ژنها
• مولکول های دیگر
بنا به تعریف موسسه ملی بهداشت آمریکا، بایومارکر (نشانگر زیستی) یک شاخص قابل اندازه گیری از وجود بیماری یا شدت آن است. در حالت کلی تر بایومارکر را می توان هر عاملی دانست که بتوان از آن به عنوان یک شاخص تعیین بیماری یا تعیین وضعیت فیزیولوژیک ارگانیسم استفاده کرد.
به بیان دقیق تر بایومارکر، تغییر در وضعیت (state) یک پروتئین است که این تغییر خود نشانگر وجود یک بیماری، ریسک پیشرفت یک بیماری و یا مثلا میزان تاثیر یک درمان خاص برای یک بیماری می باشد.
به عنوان مثالی آشنا بالا رفتن تب یک نشانگر برای سرماخوردگی و یا فشار خون بالا نشان گر احتمال وقوع سکته قلبی قلمداد می شود.
- چرا از بایومارکرها استفاده می شود؟
بایومارکرها می توانند کاربردهای متنوعی داشته باشند: تشخیص زودرس، سنجش پیشرفت بیماری و انتخاب بهترین متد درمان.
در یک تقسیم بندی کلی، بایومارکرها را می توان به دو دسته کلی: (1) بایومارکرهای مرتبط با بیماری (disease related) و (2) بایومارکرهای مرتبط با دارو (drug related) تقسیم نمود.
بایوماکرهای مرتبط با بیماری خود به دسته های زیر تقسیم می شوند.بایوماکرهای پیش بینی درمان (predictive biomarkers) که نشانگری برای احتمال میزان اثرگذاری یک درمان خاص است.بایومارکرهای تشخیصی (diagnostic biomarkers) که احتمال وجود یک بیماری در شخص را تشخیص می دهند.
بایومارکرهای پیش بینی گسترش بیماری (prognostic biomarkers) که فارغ از نوع درمان انتخابی، احتمال میزان گسترش بیماری را بررسی می کنند.در نقطه مقابل، بایومارکرهای مرتبط با دارو (drug related) این احتمال را بررسی می کند که درمان انتخابی بر یک بیمار خاص چه تاثیری خواهد گذاشت.
- چه بایومارکری، را می توان بایومارکر مناسب دانست؟
از دید علمی هر نشانگری که نتایج دقیقی(promising result) را در اختیار درمانگر قرار دهد، می تواند بایومارکر مناسبی باشد. اما به لحاظ کاربردی، می توان پارامترهایی مثل:
در دسترس بودن و قابل شناسایی مستقیم در ارگان ها یا غیر مستقیم در بزاق، خون، عرق و تنفس شخص قابلیت اندازه گیری آسان و نهایتا قابلیت کمی کردن اندازه گیری انجام شده با احتمال مورد نظر درمانگر (مثلا وقوع بیماری) را می توان مواردی دانست که یک بایومارکر را مناسب بدانیم.
- بایومارکر در سیگنال مغزی (EEG)
پس از تردیدهای بسیار و آزمون و خطای طولانی، بالاخره استفاده از بایومارکرها در تشخیص اختلالات روانی به رسمیت شناخته شد. کتاب مرجع The Diagnostic and Statistical Manual of Mental Disorders در چاپ ششم صراحتا اشاره می کند:
” تشخیص اختلال روانی نه فقط از طریق معاینه بالینی که با دانستن این که کدام سیستم مغزی دچار مشکل عملکرد شده است، هم ممکن است”.
بایومارکرهای سیگنال مغزی (EEG) راهی غیر تهاجمی و ارزان برای تشخیص یک سری اختلالات روانی در اختیار درمانگران می گذارد. به عنوان مثال در اختلالی مانند آلزایمر ، سیگنال EEG می تواند اطلاعات ارزشمندی درباره دینامیک مغز در اختیار درمانگر قرار دهد. از همین رو بایومارکرهای سیگنال مغزی می توانند نشانگر مناسبی برای تشخیص آلزایمر باشند. آلزایمر با تخریب سلول های مغزی که فعالیت طبیعی مغز را تحت تاثیر قرار می دهد، باعث عوارضی مانند تخریب حافظه و مشکلات شناختی برای شخص می شود. تاثیر آلزایمر بر سیگنال های مغزی به صورت هایی مانند کاهش سرعت EEG، کاهش همبستگی سیگنال ها (Signal Coherence)، و کاهش EEG complexity خود را نشان می دهد.همان طور که در این مثال مشخص است، بایومارکرهای مبتنی بر سیگنال مغزی می توانند در تشخیص آلزایمر موثر باشند.
به همین صورت طیفی از اختلالات بایومارکر مربوط به خود را در سیگنال مغزی دارند که می توان پس از گرفتن سیگنال مغزی کنترل نمود که وضعیت فرد درباره آن اختلال به چه صورت است.
بیومارکرهای سرطان
انواع مختلف بیومارکرهای سرطانی وجود دارد و هر یک از آنها در بدن نقش متفاوتی دارند و به روشهای مختلف واکنش نشان میدهند. به طور کلی، بیومارکرهای سرطانی به واسطه عملکردهای مختلف آنها طبقه بندی می شوند:
بیومارکرهایی که منجر به رشد و تکثیر غیر طبیعی سلولها میشوند
یک نمونه از این نوع بیومارکر، پروتئین HER2 است که به کنترل رشد سلول کمک میکند. اگر HER2 در سلولهای سرطانی بیش از حد بیان شود، سلولها HER2 مثبت در نظر گرفته میشوند، به این معنی که پروتئین بیشتری نسبت به حالت طبیعی دارند. این وضعیت احتمالا باعث میشود، سلولها سریعتر رشد کنند و شانس خود را برای متاستاز کردن (گسترش) به سایر قسمتهای بدن افزایش دهند. همچنین به این معنی است که درمانهایی که به علت اختلال در مسیر سیگنالینگ HER2 شناخته میشود، به توقف رشد سرطان کمک میکند.
بیومارکرهایی که از فعالیت درمانی سلولی یا مولکولی پشتیبانی میکنند
این نوع بیومارکر به وسیله یک ژن به نام SPARC تولید میشود که منجر به ترشح پروتئین اسیدی Cysteine-Rich میشود.SPARC به انتقال آلبومین – نوعی از پروتئین موجود در خون، سفیده تخم مرغ، شیر و سایر مواد – به سلولها کمک میکند. برخی از داروهای شیمی درمانی با آلبومین جهت جلوگیری از حل شدن در خون متصل میشوند. بنابراین، بیان بیش از حد SPARC به درمانهای مربوط با آلبومین کمک میکند و میتواند درمان سلولی موثری باشد.
بیومارکرهایی که باعث کاهش فعالیت درمانی سلولی یا مولکولی میشوند
برخی داروهای شیمی درمانی برای از بین بردن DNA تومور با پلاتین ساخته میشوند. با این حال، یک پروتئین به نام ERCC1 وجود دارد که DNA تومور را تعمیر میکند. اگر بیومارکر سطح بالای ERCC1 را در یک تومور بیمار تشخیص دهد، عاملهای مبتنی بر پلاتین برای این بیمار بسیار مؤثر نیستند.
حتی در دستههای بیومارکر فوق، انواع مختلفی وجود دارد. به عنوان مثال، مولکولهایی که سبب رشد غیر طبیعی سلول میشوند میتوانند از جهش ژنی یا از کپیهای اضافی ژن دیگری در داخل DNA تومور، ایجاد شوند.
احتیاط: ژنهای شما و بیومارکرهای سرطان شما دقیقا یک چیز نیستند.
در برخی از افراد DNA ژن قابل شناسایی وجود دارد که میتواند منجر به افزایش خطر ابتلا به سرطانهای خاص شود. به عنوان مثال، فردی که جهشهای خاصی را در BRCA1 و BRCA2 به نام “ژنهای سرطان پستان” به ارث برده است، خطر ابتلای بیشتر به سرطان پستان، تخمدان، پروستات و سایر انواع سرطان را دارد.
با این حال، اکثر سرطانها به ارث برده نمیشوند و در اکثر موارد افرادی که با سرطان تشخیص داده میشوند، هیچ کدام از ژنهای سرطان را ندارند. اما همه سرطانها دارای بیومارکرهای زیستی هستند، از جمله نشانگرهای ژنتیکی. بنابراین، تفاوت چیست؟
سرطان شما یک نسخه منحصر به فرد از DNA شما دارد که با DNA در سلولهای سالم شما متفاوت است. اکثر بیومارکرهای سرطانی که با درمان مرتبط هستند با ژنهای منحصر به فرد تومور و ساختار مولکولی، به جای ژنهای سالم، مرتبط هستند.
تشخیص و اندازهگیری بیومارکرها برای ایجاد یک برنامه درمان ضد سرطان شخصی
برای تعیین اینکه آیا و در چه سطحی، مشخصههای بیومارکرهای موجود در سرطان شما وجود دارد، پزشک شما باید یک نمونه از بافت تومور یا مایعات بدن را بیرون بیاورد و آن را به یک آزمایشگاه برای انجام یک سری از آزمایشات آسیبشناسی پیشرفته و آزمایشهای پروفایل مولکولی ارسال کند. این آزمایشات سطوح بیومارکرهای خاص خود را برای سرطان مشخص میکند. سپس اطلاعات به دست آمده با تحقیقات منتشر شده توسط محققان پیشرو در زمینه سرطان در جهان مطابقت خواهند یافت تا مشخص شود کدام درمانها به احتمال زیاد کار خواهند کرد. سپس پزشک شما یک گزارش را ارسال میکند که لیستی از عواملی را که در نمونه شناسایی شدهاند، همراه با درمانهایی که به طور مثبت و منفی مرتبط با آن عوامل شناخته شده است، نشان میدهد. این فرآیند اجازه میدهد تا پزشک شما به شخصیسازی برنامه درمان ضد سرطان شما پرداخته و درمان منحصر به بیماری شما را تدوین نماید.
بیومارکرهای استرس اکسیداتیو
استرس اکسیداتیو، قسمت سمی اکسیژن و متابولیسم را نشان میدهد. استرس اکسیداتیو به عنوان عدم تعادل بین اکسیدانها و آنتیاکسیدانها به نفع اکسیدانها شناخته شده که منجر به اختلال در سیگنالینگ مجدد، کنترل چرخه سلولی و آسیب مولکولی میشود.
بیومارکرهای استرس اکسیداتیو به سه دسته اصلی تقسیم میشوند:
- گونههای فعال اکسیژن ROS
- DNA / RNA، چربیها و پروتئینهایی که توسط اکسیداسیون آسیب دیدهاند.
- آنتیاکسیدانها
درباره این سه گروه این توضیح را باید افزود که:
- ROS نشاندهنده عواملي هستند كه استرساكسيداتيو را تحريك مي كنند و باعث آسیب به اجزاي سلول میشوند.
- آسیب DNA / RNA، پراکسیداسیون لیپید و اکسیداسیون / نیترات پروتئین، آسیبهای ناشی از اکسیداسیون را نشان میدهد.
- آنتیاکسیدانها سیستمهای مبارزه با استرس اکسیداتیو را نشان میدهند.
گونه فعال اکسیژن ROS
گونه فعال اکسیژن، گونههای شیمیایی واکنشی هستند که حاوی اکسیژن فعال میباشند. آنها عبارتند از پراکسید، سوپراکسید، هیدروکسیل رادیکال، اکسیژن مجزا و آلفا اکسیژن.
با توجه به ماهیت گذار آنها، به راحتی در سلولهای زنده با استفاده از تستهای رنگسنجی، مانند DCFDA، اندازهگیری میشوند. این بیومارکرها قابل اندازهگیری در خون، پلاسما، بافت و ادرار هستند.
آسیب DNA / RNA، پراکسیداسیون لیپید، و اکسیداسیون / نیترات پروتئین
استرس اکسیداتیو را میتوان به طور غیرمستقیم با اندازهگیری سطوح آسیب DNA / RNA، پراکسیداسیون لیپید و اکسیداسیون / نیترات پروتئین، به جای اندازهگیری مستقیم گونههای فعال اکسیژن، اندازهگیری کرد. بیومارکرهای استرس اکسیداتیو پایدارتر از انواع اکسیژن فعال هستند.
آسیب DNA / RNA
انواع مختلفی از آسیب DNA / RNA وجود دارد که میتواند به عنوان بیومارکرهای استرس اکسیداتیو اندازهگیری شود. 8-hydroxydeoxyguanosine احتمالا به عنوان یکی از رایج ترین بیومارکرهای آسیب DNA برای استرس اکسیداتیو است. تستهای مکانهای apurinic / apyrimidinic و آزمونهای آسیب ناشی از آلدهید میتواند به عنوان اندازهگیریهای مستقیم از آسیب DNA استفاده شود که به طور بالقوه مرتبط با استرس اکسیداتیو است.
پراکسیداسیون لیپید
مالوندیآلدئید MDA یکی از معمولترین شاخصهای لیپیدی استرس اکسیداتیو است. این ماده از طریق پراکسیداسیون اسیدهای چرب غیراشباع تشکیل شده است و معمولا با استفاده از آزمون TBARS اندازهگیری میشود. تست TBARS به طور کامل برای MDA خاص نیست، همانطور که سایر آلدهیدها نیز سیگنال مشابهی را با این تست تولید میکنند، با این حال، تست TBARS عموما راحتتر از استفاده از HPLC برای اندازه گیری MDA است. آزمونهای ELISA رقابتی برای MDA نیز در دسترس هستند.
دیگر بیومارکرهای پراکسیداسیون چربی شامل 4-HNA، 8-ایزوپروستان، هیدروپراکسید لیپیدها و LDL اکسید شده است.
اکسیداسیون / نیترات پروتئین
آسیب اکسیداتیو به پروتئینها میتواند به شکل کربن لیپتین پروتئین و نیتراسیون پروتئین (3-نیتروتیروزین) باشد. گونههای فعال اکسیژن همچنین میتوانند تولید محصولات پیشرفته گلیکوزیله AGE و پروتئینهای AOPP را ایجاد کنند. همه این بیومارکرها را میتوان با روشهای استاندارد اندازهگیری کرد.
آنتیاکسیدانها
آنزیمهای آنتیاکسیدانی و دیگر مولکولهای ROS، باعث آسیب اکسیداتیو می شوند. سه نوع آنتیاکسیدان به عنوان بیومارکر استرس اکسیداتیو وجود دارد: مولکولهای کوچک، آنزیمها و پروتئینها (مانند آلبومین).
برای اندازه گیری ظرفیت کلآنتی اکسیدانی نمونه، از جمله مولکولکوچک و ظرفیت آنتیاکسیدانی پروتئین، تعدادی از تستها وجود دارد. یکی از رایجترین تستهای کلسترول آنتیاکسیدانی، تست آنتیاکسیدانیTEAC است. تست آنتیاکسیدانی رادیکال اکسیژن ORAC یکی دیگر از آزمونهای معمول استرس اکسیداتیو است که ظرفیت آنتیاکسیدان را با اندازهگیری توانایی آنتیاکسیدانها برای کاهش رنگ فلورسنت توسط ROS اندازهگیری میکند.
فعالیت آنتیاکسیدانی نیز میتواند در سطح آنالیتهای خاص اندازهگیری شود. به عنوان مثال با نگاه کردن به سطوح نسبی GSH و GSSG ، سطح آنالیت اندازهگیری میشود. گلوتاتیون احیا GSH به عنوان مولکولی فراوان در میان آنتیاکسیدانهای درون سلولی در نظر گرفته میشود که GSSG را در فرم اکسید شده تشکیل میدهد. این واکنش توسط آنزیم گلوتاتیون ردوکتاز فعال میشود.
در غیر این صورت، سطح فعالیت آنزیمهای آنتیاکسیدانی مانند GST و سوپراکسیددیسموتاز میتواند در رابطه با سطوح استرس اکسیداتیو اندازهگیری شود.

