
Blog
مهندسی بافت

مهندسی بافت چیست و چه کاربردهایی دارد؟

مهندسی بافت علمی است که از ترکیب داربست، سلول و مولکول های زیستی فعال برای ساخت بافتی جهت بازسازی یا حفظ عملکرد و بهبود بافت آسیبدیده یا حتی یک اندام در آزمایشگاه استفاده میکند. پوست و غضروف مصنوعی ازجمله بافتهای مهندسی شدهای هستند که سازمان غذا و دارو آمریکا (FDA) آنها را برای استفاده بالینی تایید کرده است. در این مطلب علاوه بر تعریف مهندسی بافت به کاربردها و موفقیتهای آن، انواع داربستها و سلولهای لازم و چالشهای پیشرو به زبان ساده میپردازیم.
مهندسی بافت چیست ؟
اساس مهندسی بافت از ۳۰ سال پیش (دهه ۹۰ میلادی) تاکنون ثابت است. این فرایند با برقراری پیوند بین علم مواد و زیستشناسی، به بازسازی بافت و عملکرد اندامها کمک میکند. در مهندسی بافت، مادهای زیست تخریبپذیر که در محیط بدن خودبهخود از بین میرود، ساختاری شبیه به یکی از بافتها یا اندامهای آسیبدیده درمیآید. به ایبن ساختار داربست میگویند. سلولهای مناسب برای تشکیل بافت موردنظر روی این داربست قرار میگیرند. داربست در بدن جاندار کاشته میشود و با «تکثیر سلول ها» (Proliferation)، تشکیل اتصالات بین سلولی و در نهایت تشکیل بافت، داربست کمکم از بین میرود.
داربست در مهندسی بافت
«داربست» (Scaffolds) ساختارهایی هستند که شرایطی شبیه به ماتریکس خارج سلولی داخل بدن را برای تکثیر، رشد و اتصالات سلولها در محیط آزمایشگاهی فراهم میکنند. وظایف این ساختار به شرح زیر است.
- فراهم کردن محیطی برای اتصال، مهاجرت، رشد و «تمایز» (Differentiation) سلولها در «شرایط آزمایشگاهی» (in vitro) و «محیط داخلی بدن» (in vivo)
- فراهم کردن شکل و حمایت مکانیکی برای بافت آسیبدیده و حفظ استحکام بافت مهندسی شده
- برهمکنش فعال با سلولها برای تسهیل فرایندهای مختلف ازجمله تکثیر و تمایز
- منبع ذخیره و ناقلی برای فاکتورهای رشد
- فراهم کردن حجم کافی برای تشکیل رگ های خونی و شکلگیری بافت
ویژگیهای داربستهای مهندسی بافت
داربستها یکی از سه جزو اصلی در مهندسی بافت هستند که ساختاری سهبعدی برای انجام فرایندهای سلولی فراهم میکنند. این ساختار سهبعدی نیاز به ویژگیهای ساختاری، زیستی و مکانیکی مشخصی برای کمک به انجام این فرایندها دارد.
ویژگیهای ساختاری
داربستها باید فضای کافی برای تشکیل بافت را در اختیار سلولها قرار دهند. برای انتقال مواد موردنیاز سلول این ساختارها باید تخلخل و همزمان استحکام کافی داشته باشند. همچنین سرعت تخریب آنها باید با سرعت تشکیل بافت جدید متناسب باشد.
ویژگیهای زیستی
داربستها باید با بدن موجود زنده تعامل داشته باشند و برای فرایندهای سلولی آسیبی ایجاد نکنند. سه ویژگی زیر کمک میکنند داربست و بدن موجود زنده ارتباط بهتری برقرار کنند.
- «زیستسازگاری» (Biocompatibility)
- «زیستفعالی» (Bioactivity)
- «زیستتخریبپذیری» (Biodegradable)
زیست سازگاری
داربستها باید برای رشد، تکثیر و تمایز سلولهای گرفته شده از بدن «خود فرد» (Auotogenic)، «انسان دیگر» (Allogenic) یا سلولهای گرفته شده از «گونه های دیگر» (Xenogenic)، در محیط آزمایشگاهی و بدن انسان سازگار باشند. به این ویژگی زیستسازگاری گفته میشود. ترکیبات زیستسازگار برای سلولها و بافتهای بدن سمی نیستند و واکنشهای ایمنی و حساسیت ایجاد نمیکنند.
زیستفعالی
برای برهمکنش فعال با سلولها و مولکولهای زیستی لازم است داربستها زیستفعال باشند. برهمکنش با مولکولهای زیستی برای شکلگیری بافت، اتصالات بین سلولی، تمایز و انتقال پیامهای شیمیایی نقش مهمی دارد. همچنین داربست باید با مولکولهای فاکتور رشد سازگاری باشد و توانایی کپسوله و ذخیره کردن فاکتورهای رشد خارج از بدن را داشته باشد. برای مثال داربستهای هیدروژلی با پیوندهای کووالانسی یا یونی ساخته میشوند که پروتئین ها را در خود نگه میدارند و با جذب آب آزاد میکنند.
زیستتخریبپذیری
داربستهای زیستتخریبپذیر از موادی تشکیل میشوند که بهراحتی در بدن یا طبیعت از بین میروند و به مولکولهای غیرسمی تبدیل میشوند که دفع آنها انسان را دچار دردسر نمیکند. داربستهایی که از مواد طبیعی مثل پلیمر آلژینات ساخته میشوند این ویژگی را دارند.
ویژگیهای مکانیکی داربست
داربستها در بافتهای آسیبدیده، حمایت مکانیکی فراهم و به پایداری شکل بافت کمک میکنند. حمایت مکانیکی از آسیب بیشتر بافت جلوگیری میکند. همچنین داربست با حفظ شکل بافت به حفظ عملکرد اندام کمک میکند. مقاومت در برابر فشار و ضربه، خاصیت کشسانی و استحکام داربست باید تا حد زیادی مشابه بافت طبیعی باشد.
روشهای داربستی در مهندسی بافت
۴ روش بر اساس داربست برای مهندسی بافت گسترش یافته است. این روشها شامل موارد زیر میشوند.
- داربستهای متخلل پیشساخته که برای کاشت سلول است.
- ماتریکس خارج سلولیِ سلولزدایی شده که از بدن انسان یا گونههای دیگر گرفته میشود.
- صفحات سلولی که همراه ماتریکس خارج سلولی ترشح شده از سلول است.
- هیدروژلهای حاصل از خودآرایی که سلولها را کپسوله میکنند.
داربست متخلخل پیشساخته
داربستها در این روش معمولا از مواد زیستتخریبپذیر ساخته میشوند، سلولها روی آن قرار میگیرند و سپس در بافت یا اندام موردنظر پیوند داده میشوند. مسئله اصلی در استفاده از داربستهای سنتزی ویژگی زیستسازگاری آنها است. به همین دلیل از فرایندهای مختلفی برای ایجاد تغییرات سطحی و افزایش زیستسازگاری در این داربستها استفاده میشود. ترکیبات سازنده این داربستها از دو دسته مواد معدنی و آلی تشکیل شده است.
ماتریکس خارج سلولیِ سلولزدایی شده
این ماتریکس طبیعیترین نوع داربست برای مهندسی بافت است. در این روش تمام مواد و سلولهای ایمنیزا برداشته میشوند و داربست ماتریکس دستنخورده باقی میماند. روشهای سلولزدایی باید برای بافتهای مختلف بهینه شوند تا کمترین تغییر در ویژگیهای مکانیکی و بیوشیمیایی ماتریکس خارج سلولی بهوجود بیاید. برای سلولزدایی این داربست، ترکیبی از روشهای فیزیکی، شیمیایی و آنزیمی استفاده میشود.
- قبل از جدا کردن ساختارهای ماتریکس خارج سلولی، غشای پلاسمایی بهوسیله روشهای فیزیکی «چرخه انجماد و ذوب» (Freeze-Thaw Cycles) یا محلول های یونی از بین میرود.
- با از بین رفتن غشا، بخشهای سیتوپلاسمی و هسته ای، محلول و بهوسیله دترجنتها و روشهای آنزیمی ازجمله تریپسین/EDTA جدا میشوند.
این داربستها ساختارهایی مثل ماتریکس خارج سلولی هستند که از قبل ساختار مشخصی دارند و با تغییراتی برای استفاده آماده میشوند. از دید نظری، این داربستها برای مهندسی بافت در اولویت هستند، چون زیستسازگاری بالایی دارند و رشد و اتصال سلول را بهراحتی تسهیل میکنند. اما استفاده از آنها مشکلات زیر را ایجاد میکند.
- پایداری فیزیکی و مکانیکی این داربستها کم است به همین دلیل برای بافتهای تحت فشار، مناسب نیستند.
- ممکن است بدن آنها را بهعنوان آنتی ژن بشناسد و سیستم ایمنی را فعال کنند.
صفحات سلولی با ترشح ماتریکس خارج سلولی
در این روش سلولها با اتصال بههم، ماتریکس خارج سلولی خود را ترشح میکنند و بدون هیچ واکنش آنزیمی در بدن کاشت میشوند. سلولها در این روش تا قبل از اتصال، در ظرفی با کف پوشیده شده از پلیمر حساس به دما مثل پلیایزوپروپیل آکریلآمید، کشت داده میشوند. صفحه سلولی بهوسیله تغییر آبگریزی پلیمر، با تغییر دما از سطح ظرف جدا خواهد شد. این داربستها برای تشکیل بافت های پوششی اندوتلیال و اپیتلیال بسیار مناسب هستند.
کپسوله کردن سلول در ماتریکس هیدروژلی
«کپسوله کردن» (Encapsulation) فرایند بهدام انداختن سلول زنده در یک غشای نیمه تراوا یا تودهای همگن است. هیدروژلها، پلیمرهایی هستند که با اتصال عرضی یا کووالانسی به هم متصل شدهاند و توانایی جذب آب بالایی دارند. در کپسوله کردن سلولها بیشتر ازداربستهای هیدروژلی استفاده میشود. پلیمرهای طبیعی کلاژن و ژلاتین توانایی تشکیل هیدروژل دارند.
هیدروژل ترمیم زخم
مزایای استفاده از داربست متخلخل پیشساخته
استفاده از این روش برای ساخت بافت مهندسی شده مزایا و معایبی دارد که در جدول زیر بررسی میکنیم.
| مزایا | معایب |
| تنوع زیاد مواد زیستی پیشساز داربست | زمانبر بودن کاشت سلول در داربست |
| امکان طراحی دقیق ساختار اصلی و ریزساختارها | عدم پخش یکنواخت سلولها روی داربست |
| امکان کنترل خصوصیات فیزیکی و شیمیایی | یکنواخت نبودن ویژگیهای بافت تشکیل شده |
| هزینه زیاد داربست | |
| مرگ تعداد زیاد سلولهای قرار گرفته روی داربست |
روشهای ساخت داربست
برای مهندسی بافتهای مختلف، داربستهایی با مقاومت، انعطافپذیری و تخلخل متفاوت نیاز است. برای رسیدن به این هدف، از روشهای متنوعی برای ساخت داربستها استفاده میشود.
- «نمونهسازی سریع» (Rapid Prototyping)
- «چرخش یا اسپری الکتریکی» (Electrospinning/Electrospraying)
- «مهندسی فراساختار» (Superstructure Engineering)
- «قالبگیری حلال یا تصفیه مواد تخلخلساز» (Solvent Casting/Porogen Leaching)
- «خشکشدن انجمادی» (Freeze-drying)
- «جدایی فاز» (Phase Separation)
- «کفزایی گازی» (Gas Foaming)

روش نمونهسازی سریع
نمونه سازی سریع(3D printing)
نمونهسازی سریع، مجموعهای از روشها است که بهوسیله پلیمرها و از روی الگوی کامپیوتری، داربست سهبعدی را لایهلایه چاپ میکند. برخلاف روشهای سنتی، مماده کمتری مصرف میشود و هدرفت کمتری هم داریم. اما ساختارهایی با صحت، دقت و تکرارپذیری طراحی میشود. جوهر در این نوع چاپ، پلیمرهای بیشکل یا کریستاله شده ازجمله پلی کاپرولاکتون (PCL)، پلیلاکتیکاسید (PLA)، پلیلاکتیک کو-گلیکولیکاسید (PLGA) و پلیونیل الکل (PVA) است.
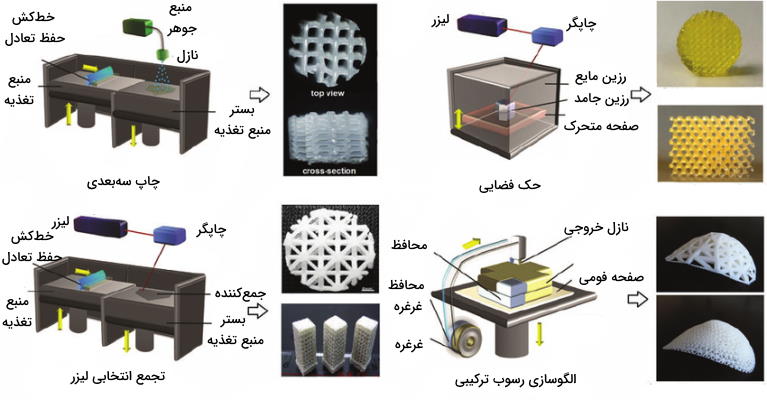
چرخش یا اسپری الکتریکی
«الکتروریسی» (Electrospinning) یکی از پرطرفدارترین روشهای ساخت داربستهای مهندسی بافت است. در این روش به کمک محلول پلیمر (سنتزی یا طبیعی) و میدان الکتریکی داربستهایی با فیبرهایی با قطر نانو یا میکرو و طول چندمتری ساخته میشود که ساختاری «توری شکل» (Meshwork) دارند. تخلخل و قطرفیبرها در این روش با تغییر عوامل زیر کنترل میشود.
- غلظت پلیمر
- ولتاژ میدان الکتریکی
- فاصله بین نازل و صفحه جمعکننده

مهندسی فراساختار
«خودتجمعی» (Self-assembly) به معنی قرار گرفتن اجزای سازنده یک ساختار بدون حضور الگوی آماده و به کمک نیروهای بینمولکولی فاصلهکوتاه ازجمله نیروهای غیرکووالانسی، واندروالسی و همچنین برهمکنشهای یونی، آبگریز و مغناطیسی است. استفاده از این روش مزایای زیادی دارد.
- با استفاده از این روش میتوان ساختار داربست را در سطح مولکولی کنترل کرد و ساختاری پیچیده طراحی کرد که بیشترین شباهت به محیط داخل بدن را دارد.
- خاصیت خودترمیمی این داربستها را برای استفاده در محیطهای با فشار بالا، مناسب میکند.
- میتوان مولکولها را به صورت هیدروژل به بیمار تزریق کرد تا داربست در داخل بدن ساخته شود.
قالبگیری حلال یا تصفیه مواد تخلخلساز
قالب گیری محلول (SCPL) یکی از روشهای ساده و کمهزینه برای ساخت داربستهای با تخلخل زیاد است. در این روش مادهای جامد، مایع یا گاز در محلول پلیمری پخش میشود و با تصعید، تبخیر یا ذوب آن، منافذی در پلیمرِ شکلگرفته بهجا میماند. به کمک این روش میتوان داربستهایی با تخلخل ۹۰٪ و منافذی با بیشترین قطر ۵۰۰ میکرومتر ساخت. اندازه منافذ و درصد تخلخل داربست در این روش را میتوان با تغییر غلظت و مقدار پلیمر و ماده «تخلخلساز» (Porogen) تنظیم کرد. استفاده از این روش معایبی هم دارد.
- شکل و سایز منافذ در این روش یکدست نیست.
- ارتباط بین منافذ در این روش کم است.
- در این روش از پلیمرهای معدنی استفاده میشود که احتمال «سمیت سلولی» (Cytotoxicity) را افزایش و برهمکنش با مولکولهای زیستی را کاهش میدهد.
- داربستهایی که با این روش ساخته می شوند، خواص مکانیکی لازم برای بافتهای تحت فشار را ندارند.
خشکشدن انجمادی
در این روش بهوسیله انجماد و تصعید، از محلول آبی یا آلی پلیمر، داربستهایی با تخلخل زیاد ساخته میشود. این روش برای استفاده از پلیمرهای حساس به دمای بالا و برای صفحات داربست سهبعدی مناسب است. ساختار داربست بهوسیله تغییر در پارامترهای زیر کنترل میشود.
- وزن مولکولی پلیمر
- غلظت پلیمر
- ویسکوزیتی محلول پلیمر
- نوع حلال
- سرعت کاهش دما
- دمای انجماد
کاهش دمای محلول با سرعت زیاد، منافذ یکدستتر ایجاد میکند. همچنین کاهش دمای انجماد، میانگین اندازه منافذ را کاهش میدهد.
جدایی فاز
جدایی فاز با جدا کردن بخش حلال و پلیمر از روشهای مختلف، ساختارهای منفذداری میسازد که در مهندسی بافت و دارورسانی کاربرد دارند.
- اضافه کردن غیرحلال: جدایی فاز با اضافه کردن مادهای «غیرحلال» (Nonsolvent) به محلول پلیمری انجام میشود. با این روش میتوان داربستهایی با منافذ ناهمگن از نظر اندازه و شکل ساخت. چون مهندسی بافت نیاز به داربستهایی با منافذ یکدست دارد، این روش کاربرد زیادی ندارد.
- افزایش دما: در این روش با تغییر دمای جزئی محلول، پایداری ترمودینامیکی پلیمر تغییر میکند و پلیمر و حلال در دو فاز مختلف قرار میگیرند و از هم جدا میشوند. در مرحله بعد، حلال بهوسیله تبخیر یا خشکشدن انجمادی خارج میشود و پلیمر داربستی با تخلخل و ارتباط بین منافذ مناسب تشکیل میدهد.
ساختار داربست و اندازه و شکل منافذ آن، با تغییر وزن مولکولی و غلظت پلیمر، نسبت حلال به حلشونده و روشهای سرد کردن کنترل میشود. منافذ داربستها در این روش، در مسیرها خروج حلال بهوجود میآیند. به همین دلیل ارتباط داخلی آنها حفظ میشود و آنها را به یکی از گزینههای مناسب برای مهندسی بافت تبدیل خواهد کرد.
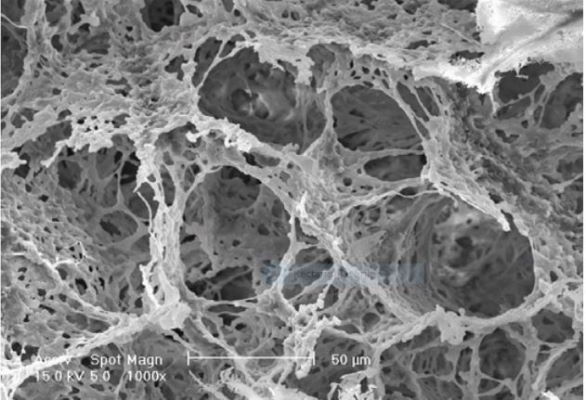
کفزایی گازی
کفزایی گازی بدون دخالت حلال و با استفاده از اثر گسترش گاز، داربستهایی با تخلخل زیاد میسازد. دیاکسید کربن (CO2) گازی ایمن، قابل استفاده مجدد و از نظر هزینه به صرفه است که در این کاربرد دارد. مراحل انجام این روش در زیر آمده است.
- پلیمر با گاز CO2 فشار بالا، اشباع میشود.
- با کاهش کنترل شده فشار، مولکوهای CO2 کنار هم قرار میگیرند و حباب تشکیل میدهند.
- حبابها خارج میشوند و داربست متخلخل تشکیل میشود.
داربست مهندسی بافت از چه موادی ساخته میشود؟
داربستهای مهندسی بافت از مواد معدنی و آلی ساخته میشوند. سرامیک یکی از مواد معدنی پرکاربرد در ساخت داربستها است که به دلیل ویژگیهای مکانیکی که دارد (تحمل فشار بالا و سختی زیاد) در مهندسی بافتهای سخت مثل استخوان کاربرد بیشتری دارد. مواد آلی به دو دسته پلیمرهای طبیعی و سنتزی تقسیم میشوند که بیشتر در مهندسی بافتهای نرم مثل ماهیچه قلب از آنها استفاده میکنند.

خصوصیتسنجی داربستهای مهندسی بافت
برای رسیدن به بهترین نتیجه در مهندسی بافت ویژگیهای شیمیایی، وزن مولکولی، حساسیت دمایی، «ریختشناسی» (Morphology) سطح و ویژگیهای مکانیکی داربستها قبل از استفاده باید ارزیابی و خصوصیتسنجی شوند. برای سنجش این ویژگیها از روشهای زیر بهره میبریم.
ویژگیهای شیمیایی: برای بررسی ویژگیهای شیمیایی و بررسی پیوندها، اتصال عرضی و «عاملی شدن سطح» (Surface Modification) داربست از چند روش معمول استفاده میکنیم.
- طیف سنجی رزونانس مغناطیسی هسته (NMR)
- طیف سنجی مارون قرمز (FTIR)
- کروماتوگرافی گاز-مایع
- طیف سنجی رامان
تعیین وزن مولکولی: وزن مولکولی پلیمر پیشساز به کمک دو روش اندازیگیری میشود.
- طیف سنجی جرمی
- کروماتوگرافی ژلی
حساسیتهای دمایی: نقطه ذوب و دمای تبدیل شیشه (Tg) پلیمر پیشساز با دو روش اندازهگیری میشود.
- «کالریمتری افتراقی» (Differential Scanning Calorimetry | DSC)
- «آنالیز توزین حرارتی» (Thermogravimetric analysis | TGA)
ریختشناسی سطح: برای بررسی ساختار سطح داربست، اندازه و شکل منافذ و قطر فیبرهای آن بیشتر از دو نوع میکروسکوپ استفاده میکنیم.
- میکروسکوپ الکترونی نگاره (SEM)
- میکروسکوپ نیروی اتمی (AFM)
ویژگیهای مکانیکی: برای ارزیابی ویژگیهای مکانیکی داربستها و پلیمر سازنده آنها ازجمله تحمل فشار، خاصیت کشسانی و ویسکوزیته از روشهای زیر استفاده میکنیم.
- «جریان شناسی» (Rheology)
- «آزمون کشش» (Tensile Testing)
- «آزمون تراکمی» (Compressive Testing)
راکتور زیستی چیست ؟
راکتور زیستی (Bioreactor) محفظهای میکروبزدایی شده یا استرلیزه است که شرایط لازم برای واکنشهای زیستی ازجمله دما، مواد غذایی، مولکولهای پیام و pH را فراهم میکند. این دستگاه در مهندسی بافت شرایط لازم برای تکثیر، رشد و تمایز بافت در محیط آزمایشگاه را در اختیار پژوهشگران قرار میدهد.
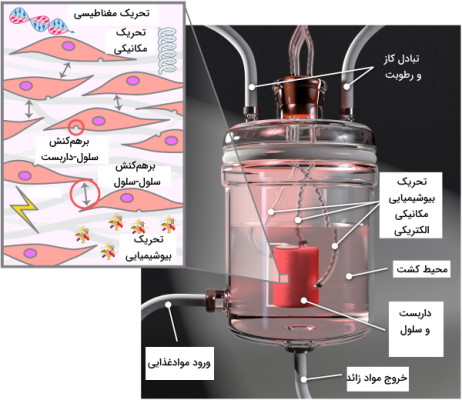
سلولها و مهندسی بافت
ساخت بافت مهندسی شده در محیط آزمایشگاهی نیاز به تکثیر، رشد و تمایز سلولها دارد. از دو دسته سلول در مهندسی بافت استفاده میشود.
- سلولهای فرد بیمار: در این روش از سلولهای بالغی استفاده میشود. سلولهای بالغ فرد فقط رشد میکنند و تکثیر میشوند. این سلولها، توانایی تمایز ندارند. برداشت این سلولها با روشهای تهاجمی است و ممکن است با درد و آسیب بیمار همراه باشد. به علاوه، محیط این سلولها بسیار تخصصیافته است و اغلب بازسازی آن در محیط آزمایشگاهی را دشوار میکند.
- سلولهای بنیادی: سه دسته از سلول های بنیادی در مهندسی بافت استفاده میشود.
- سلولهای بنیادی جنینی
- سلولهای بنیادی مزانشیمی در مغز استخوان
- سلولهای بنیادی مزانشیمی در نخاع
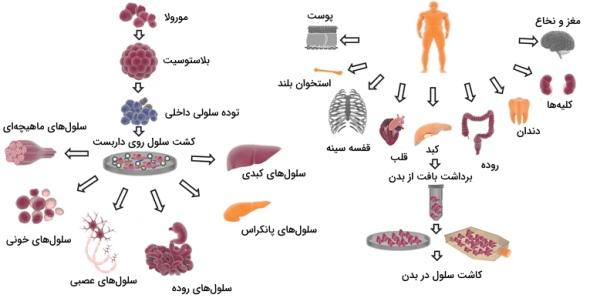
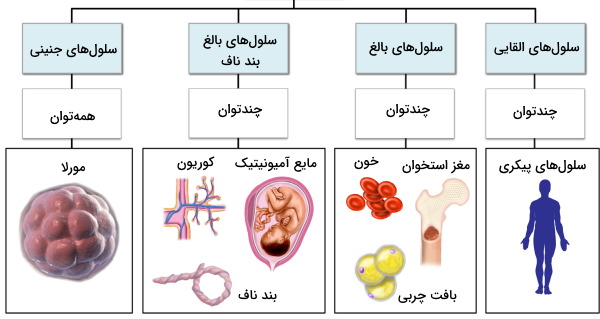
سلولهای بنیادی جنینی
سلولهای بنیادی جنینی «همهتوان» (Pluripotent) هستند و به همه ردههای سلولی تمایز مییابند. به علاوه، این سلولها میتوانند بافتهایی کاملا یکسان با بافت فرد بسازند. برای استفاده از این سلولها در مهندسی بافت باید اطمینان حاصل شود که سلولهای تمایزیافته روی داربست قرار میگیرند.
سلولهای بنیادی مغز استخوان
سلولهای بنیادی مغز استخوان «چندتوان» (Multipotent) هستند و به ردههای سلول های خونی و سلولهای استخوانی و غضروفی تمایز پیدا میکنند.
سلولهای بنیادی نخاع
سلولهای بنیادی نخاع مثل مغزاستخوان سلولهای چندتوان هستند. این سلولها به سلولهای چربی، استخوانی، کبدی و سلولهای شبیه به نورون ها تمایز مییابند.
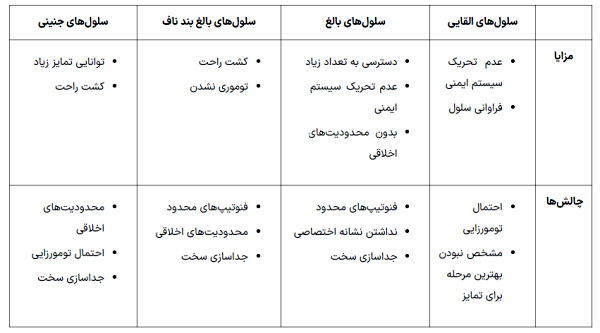
مزایا و چالشهای استفاده از هر نوع سلول در مهندسی بافت در جدول زیر آمده است.
کاربرد مهندسی بافت در حوزه های مختلف
مهندسی بافت در حوزههای مختلف، کاربردهای متنوعی دارد که در ادامه به آنها اشاره میکنیم.
مهندسی بافت قلب
بیماریهای قلبی یکی از دلایل پیشتاز در مرگ و میر سالانه کشورها است. این بیماریها ممکن است انقباض ماهیچه قلب یا خونرسانی به آن را مختل کنند. درمان این بیماریها به دلیل تنوع زیاد عوامل ایجادکننده، از فنرگذاری رگ تا پیوند قلب را شامل میشود. به همین دلیل این بیماریها توجه زیادی برای استفاده از درمانهای مهندسی بافت را به خود جلب کردهاند. چند نمونه از این روشهای درمانی در زیر آمده است.
- رگهای مهندسی بافت شده در درمان تصلب شرایین
- پیوند داربست حاوی سلولهای بنیادی در «بافتهایی با مشکل نارسایی خون» (Ischemic Tissue)
- دریچه قلب مصنوعی
- پمپ ایجاد کننده ضربان
- جایگزینی بطن در «سندرم رشد ناکامل قلب چپ» (Hypoplastic Left Heart Syndrome)
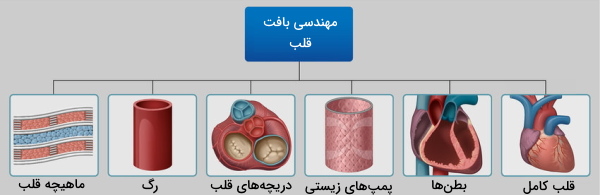
ساخت یک بافت قلب مهندسی شده، علاوه بر اصول اولیه مهندسی بافت، نیازمند در نظر گرفتن نکات زیر است.
- یکی از مهمترین مواردی که باید در مهندسی بافت قلب رعایت شود، ساخت داربستی است که توانایی انتقال جریان الکتریکی به بافت میزبان را داشته باشد.
- بافت قلب، فشار کششی زیادی را تحمل میکنند به همین دلیل پلیمری که برای ساخت داربستهای این نوع بافت استفاده میشوند باید خاصیت کشسانی زیادی داشته باشد.
یکی از بهترین روشهای ساخت داربست، برای مهندسی بافت قلب الکتروریسی است. ترکیب پلیمر پلی گلیسرول سباتات و پلی لاکتیک اسید داربستی با خصوصیات فیزیکی، شیمیایی و مکانیکی مناسب برای مهندسی این بافت ایجاد میکند.

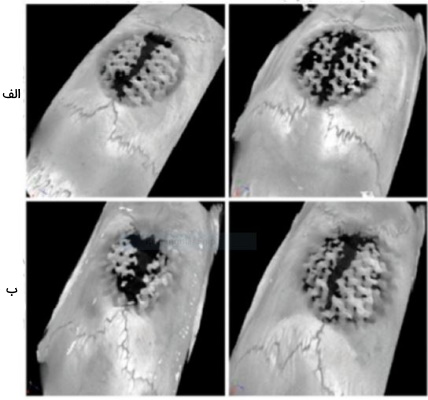
مهندسی بافت استخوان
در مهندسی بافت استخوان، تخلخل داربست یکی از ویژگیهای کلیدی برای رسیدن به بافت عملکردی است. منافذ داربست برای اتصال سلولها، تکثیر و مهاجرت آنها بسیار مهم هستند . ارتباط داخلی آنها با هم، در انتشار اکسیژن، حرکت مواد غذایی، حرکت مواد زائد و رگزایی حیاتی است. «سازه پیوندی» (Graft) بافت استخوان مهندسی شده از سه بخش تشکیل میشود.
- سلولهای استخوانی استئوبلاست و استئوکلاست: استئوبلاستها پیشسازهای کلاژنی ماتریکس استخوان را میسازند و استئوکلاستها استخوانها را برای ایجاد ساختار متخلخل میشکنند.
- فاکتورهای رشد: گروهی از فاکتورهای رشد به نام «پروتئینهای ریختزایی استخوان» (Bone Morphogenic Proteins |BMP) در مهندسی بافت استخوان استفاده میشوند.
- داربست: داربست باید تخلخل و استحکام مناسب داشته باشد.
مهندسی بافت عصبی
از آنجا که بافت عصبی ترمیم نمیشود، مهندسی بافت چشمانداز جدیدی برای این بافت بهوجود آورده است. بزرگترین چالش در این مسیر، نهتنها دست یافتن به ویژگیهای مکانیکی مناسب بلکه ارسال پیام و رشد مخروط آکسونی به دورترین اندامها است. در مهندسی بافت مغز، حفظ سد خونی-مغزی و بافت سالم فرد در اولویت است. داربست مناسب برای مهندسی بافت عصبی باید ویژگیهای زیر را داشته باشد.
- تخلخل ۹۰ درصدی
- زیستسازگاری
- زیستتخریبپذیری
- هدایت عصبی
- القای عصبی
- مقاومت در برابر عفونت
- انعطاف
مهندسی بافت پوست
پوست انسان از سه لایه اپیدرم، درم و اندودرم تشکیل شده است. هر یک از این قسمتها بافتهای متفاوتی دارند که برای عملکرد کامل پوست ضروری هستند. برای مهندسی بافت پوست قسمت یا تمامی این لایهها بازسازی میشوند. در مهندسی این بافت، باید علاوه بر سلولهای پوستی پوستی، رگها را نیز در نظر گرفت. در استفاده از داربستهای مهندسی توجه به نکات زیر ضروری هستند.
- فراهمکردن لایه محافظتی برای بازسازی کراتینوسیت
- اتصال محکم به درم پایینی
- بازسازی رگهای خونی در محل آسیب
- انعطافپذیری کافی
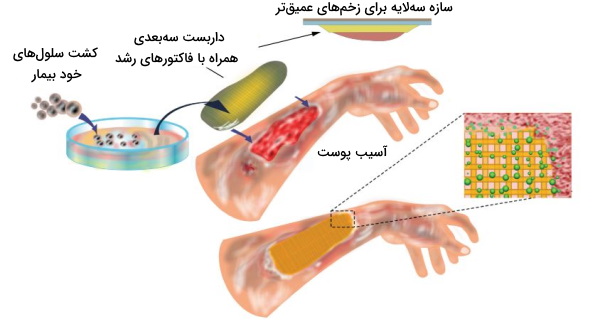
نوع بافت پوستی مهندسی شده بر اساس میزان آسیب متفاوت است و به داربستهایی با ویژگیهای زیر نیاز دارد.
- ترمیم لایههای پوستی: براساس عمق جراحت ممکن است یک یا چند لایه از پوست به ترمیم نیاز داشته باشد.
- اپیدرم: برای ترمیم این بخش، داربست حاوی سلولهای کراتینوسیت کاشته شده روی لایهای از فیبروبلاست جوندگان است. کراتینوسیتهای گرفته شده از خود بیمار به مدت ۲ تا ۳ هفته کشت داده میشوند و در صفحات ۲ تا ۸ لایه روی داربست قرار میگیرند.
- درم: بیشتر داربستهای ترمیم درم فاقد سلول و فقط ساختاری برای سازماندهی سلولها و رگزایی بافت میزبان هستند.
- اپیدرم-درم: داربستهای ترمیم اپیدرم-درم باید ویژگیهای مربوط به دو بخش بالایی پوست را داشته باشند. هر دو رده سلولی کراتینوسیت و فیبروبلاست روی این داربستها کاشته میشود. برهمکنشهای بین این دو رده سلولی مولکولهایی سبب فعال شدن مولکولهایی میشود که پوست را ترمیم میکنند.
- داربست سهلایه: این سازهها از بافت چربی، بافت اپیدرم و درم تشکیل و برای ترمیم زخمهای عمیق پوستی استفاده میشوند. بافت چربی شامل سلولهای چربی، کلاژن IV، سلولهای اندوتلیال رگها و ماکروفاژهای بافت چربی میشوند.
- رنگدانهدار شدن پوست: رنگدانههای پوست (ملانین) از سلولها در برابر اشعه فرابنفش خورشید محافظت میکنند. سازههای پیوندی این نوع درمان از سلولهای کراتینوسیت، فیبروبلاست و ملانوسیت تشکیل میشوند. رنگدانهدار شدن مجدد پوست در این نوع درمان ۳ تا ۵ هفته طول میکشد.
- رگزایی: از این سازههای پیوندی در موارد آسیب عمقی پوست، استفاده میشود. برای استفاده از سازههای پیشساز همراه با رگ، نیاز است این رگها بتوانند با رگهای طبیعی بدن ارتباط برقرار کنند. در این نوع درمان میتوان از گرفت سلولهای اندوتلیایی یا سلولهای بنیادی برای رگزایی پس از پیوند داربست و در بدن بیمار بهره برد.
زیستمواد ساخت داربست در مهندسی بافت پوست
انتخاب مواد اولیه مناسب یکی از حیاتیترین موارد در ساخت داربستهای مهندسی بافت است. ازآنجایی فشار زیادی به پوست وارد میشود، در ساخت داربستهای بازسازی پوست، علاوه بر اصول اولیه، ویژگیهای مکانیکی اهمیت بالایی دارند. بر این اساس در ساخت این داربستها از پلیمرهای زیر بیشتر استفاده میشود.
- ابریشم طبیعی
- هیالورونیک اسید
- فیبرین
- کلاژن
مهندسی بافت غضروف
بافت غضروف یکی از بافتهایی است که توانایی خودترمیمی ندارد. به همین دلیل توسعه روشهایی که به جایگزینی یا ترمیم این بافت کمک میکنند از اهمیت بالایی برخوردار است. مهندسی این بافت مثل بافتهای دیگر از سه بخش تشکیل میشود.
- منبع سلولی
- داربستها
- مولکولهای زیستی
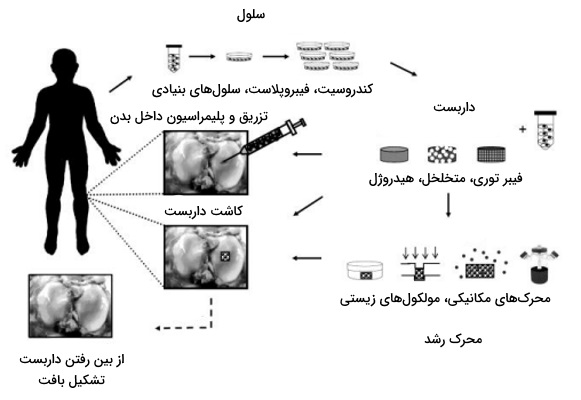
منبع سلولی مهندسی بافت غضروف
منابع سلولی که تا به امروز در مهندسی این بافت استفاده شده است، شامل سلولهای زیر میشود.
- کندروسیتها: این سلولها در بافت غضروف طبیعی وجود دارند.
- فیبروبلاستها: دسترسی به این سلولها راحت است و میتوانند به سلولهای کندروسیت تبدیل شوند.
- سلولهای بنیادی: این سلولها امکان تمایز به بسیاری از ردههای سلولی را دارند و میتوانند به کندروسیت تمایز یابند.
داربستهای مهندسی بافت غضروف
در طراحی داربستها، تراکم سلولها و نحوه کاشت آنها برای داشتن اتصالات بین سلولی کافی، باید به دقت در نظر گرفته شود. داربستهای متنوعی برای مهندسی این بافت استفاده میشود، اما داربستهای پلیمری با سه نوع ساختار، توجه بیشتری را به خود جلب کرده است.
- هیدروژلها: این داربستها به محل موردنظر تزریق میشوند یا در اندام کاشته میشوند. ساختار این داربستها تبادل مولکولهای لازم برای رشد را تسهیل میکند. برای ساخت داربستهای هیدروژلی در مهندسی بافت غضروف از مواد زیر استفاده میشود.
- پلیاتیلن گلایکول
- هیالورونیکاسید
- فیبرین
- کلاژن
- آلژینات
- داربستهای اسفنجی یا متخلخل: ویژگیها این داربستها به اندازه، تعداد منافذ و ارتباط بین منافذ بستگی دارد. پلیمرهای زیر برای ساخت این داربست مشارکت دارند.
- کیتوزان
- پلیاوکتان دیاُل سیترات
- ابریشم طبیعی
- فیبرهای توری: داربستهای توری، شبکهای از الیاف هستند که میزان تخلخل آنها، قطر فیبرها و جهتگیری آنها، رفتار سلول را تعیین میکند. معمولترین پلیمرهایی که در ساخت این داربستها استفاده میشوند، پلیهیدروکسی استرها هستند.

مولکولهای زیستی در مهندسی بافت غضروف
مولکولهای زیستی یکی دیگر از سه ضلع مهندسی بافت هستند که تشکیل غضروف را القا میکنند و افزایش میدهند. ازآنجا که بسیاری از غضروفها وابسته به نیروهای مکانیکی هستند، برای القای رشد و تمایز آنها از محرکهای مکانیکی نیز استفاده میشود.
محدودیتهای مهندسی بافت
این رشته در حال حاضر با محدودیتهایی در مورد سلولها و داربستها روبهرو است که برای ادامه کار و استفاده بهینه از این رشته باید برطرف شوند.
- یکی از محدودیتهای اصلی در مهندسی بافت، انتخاب سلول مناسب است. جداکردن سلولهای اصلی بدن فرد و کشت آن در آزمایشگاه برای مدت طولانی با مشکلات زیادی همراه است. این سلولها در شرایط محیط کشت حساسیت بالای دارند و بعد از چند تقسیم پتانسیل تمایز خود را از دست میدهند.
- ایمپلنتهای مهندسی بافت در مدلهای حیوانی واکنشهای ایمنی، عفونت، التهاب و پسزدن نشان دادهاند.
- ساخت داربستهایی که ساختار و فعالیتهای ماتریکس خارج سلولی طبیعی در بافت را با بیشترین شباهت تقلید کنند، سمیت سلولی نداشته باشند و بهراحتی استرلیزه شوند، فرایند دشواری است.
- رگزایی در سازههای بافتی بزرگ هنوز یک مشکل حل نشده است.
- در مطالعات اخیر احتمال ایجاد تومور در بافتها مطرح میشود.
جدول زیر چهار روش جایگزینی بافت آسیبدیده را با هم مقایسه میکند.
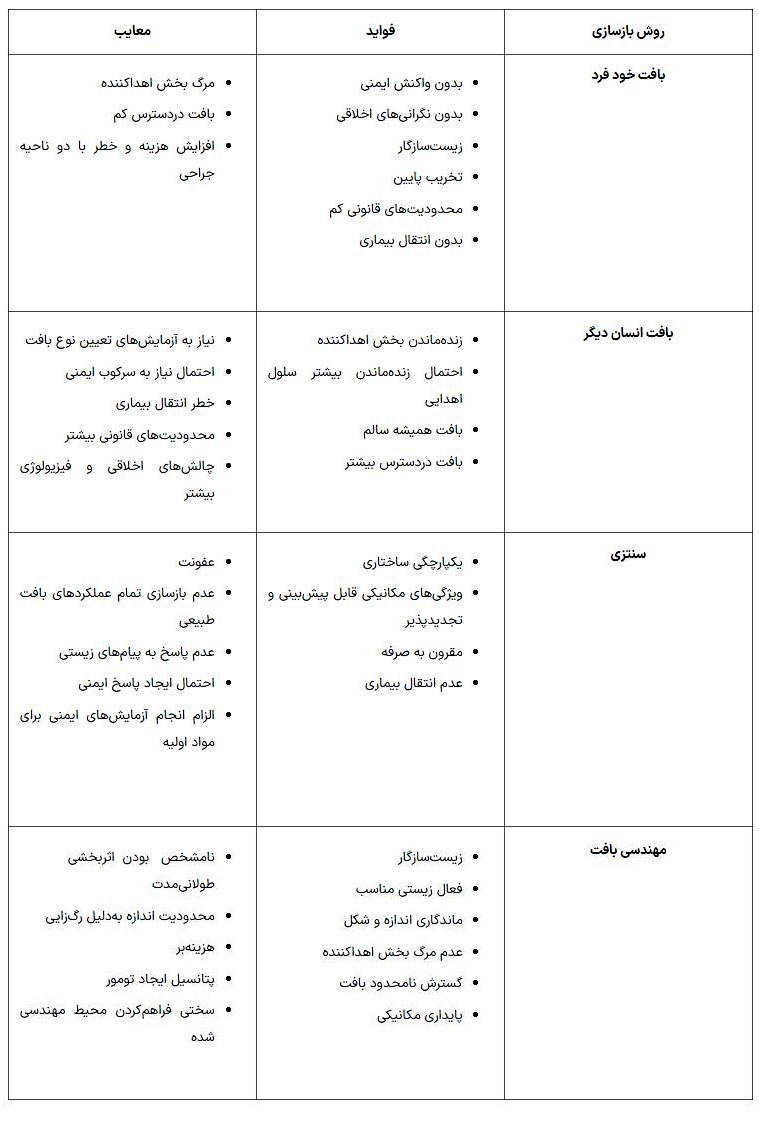
چرا مهندسی بافت مهم است؟
مهندسی بافت بزودی به بازاری تبدیل خواهد شد که نیازهای دنیای پزشکی در ازکارافتادگی اندام و آسیب بافتها را برطرف می کند و ترمیم بافتهایی را ممکن میسازد که به دلیل تمایز بازسازی نمیشوند. مهندسی بافت میتواند تحولی بزرگ در درمان بیماریها و اختلالت مختلف ایجاد و فرایند درمان را آسانتر کند. از طرفی سالانه تعداد قابل توجهی از بیماران نیازمند پیوند به دلیل نبود مورد مناسب، از دست میروند. بازسازی اندامها بهوسیله مهندسی بافت میتواند زمان انتظار پیوند را در این بیماران کاهش دهد.
تفاوت مهندسی بافت و پزشکی بازساختی
می توان گفت مهندسی بافت زیرمجموعهای از «پزشکی بازساختی» (Regenerative Medicine) است. مهندسی بافت فرایندی است که نیاز به سه جز سلول، داربست و مولکولهای زیستی فعال دارد، در حالیکه پزشکی بازساختی افزون بر مهندسی بافت، خودترمیمی بافت به کمک ساختارها و مولکولهای خود فرد یا خارجی، برای بازسازی بافت و اندام را دربرمیگیرد.
کاربرد نانوفناوری در مهندسی بافت
نانوفناوری به ساخت داربستهای مهندسی بافت کمک میکند. ساختارهای نانویی با ویژگیهای بیوشیمیایی، مکانیکی و الکتریکی که دارند، محیط بافت در بدن را تقلید و شرایط رشد را برای سلولها فراهم می کنند. این بخش کاربرد نانوساختارها در مهندسی ۳ بافت زیر را توضیح میدهد.
- بافت دندان
- بافت عصبی
- استخوان
کاربرد نانوساختارها در مهندسی بافت دندان
به دلیل اینکه آسیبهای وابسته به لثه با افزایش سن افزایش و خودترمیمی بافت دندان کاهش می یابد، درمانهای موثر برای ترمیم بافت آسیبدیده بسیار ضروری است. کمک گرفتن از مهندسی بافت، یکی از درمانهای جایگزین در ترمیم بافت لثه است. مهندسی بافت دندان بر موارد زیر تمرکز میکند.
- هدایت بازسازی بافت
- مهار عفونتهای باکتریایی
- دارورسانی بافت لثه
- تشکیل سیمان دندان
کاربرد نانوساختارها در مهندسی بافت عصبی
امروزه جراحی و پیوند بافت خود فرد یا پیوند بافت انسانی، درمانی است که برای عصب آسیبدیده استفاده میشوند. از معایب این روشها میتوان به ایجاد پاسخ ایمنی، عدم درمان کامل و تکرار جراحیها اشاره کرد. مهندسی بافت برای ترمیم بافت عصبی دو روش دارد.
- استفاده از داربستهای مناسب برای ایجاد ماترکیس بین سلولی و فراهم کردن محیط رشد سلول
- استفاده از داربست همراه با سلول برای رشد، تمایز و جایگزینی سلولهای از دست رفته
کاربرد نانوساختارها در مهندسی بافت استخوان
تمرکز مهندسی بافت استخوان درحال حاضر بر ساخت داربستهای سهبعدی است که بافت استخوانی را مثل محیط طبیعی بازسازی و حمایت کنند. ویژگیهای مکانیکی و تخلخل در این نوع داربستها بسیار مهم است. نانومواد طبیعی به دلیل ویژگیهای زیستسازگاری، زیستتخریبپذیری و معدنیسازی، از بهترین مواد ساخت داربست هستند. ویژگی زیستتخریبپذیری این مواد نیاز به جراحی ثانویه برای خروج ایمپلنت را از بین میبرد.
نانولههای کربنی در مهندسی بافت
«نانولولههای کربنی» (Carbon Nanotubes) جریان های الکتریکی را از خود عبور میدهند، از نظر شیمیایی پایدار هستند و استحکام مناسبی دارند. به همین دلیل از آنها به عنوان داربست در مهندسی بافت استفاده میشود. سطح این ساختارها قبل از استفاده در محیط کشت و ارتباط با سلول، باید عاملی شود. در این بخش، عملکرد نانولولههای کربنی در بافتهای زیر را توضیح میدهیم.
- بافت استخوانی: مطالعات انجام شده در دهههای اخیر نشان میدهد، نانولولههای کربنی داربستی مناسب برای پیوند سلولهای استئوبلاست و استئوکلاست و بازسازی بافت استخوان هستند. ساختار محکم این نانولولهها شرایط مکانیکی لازم برای تشکیل بافت استخوان و ادغام بافت جدید با بافت طبیعی را فراهم میکند.
- بافت عصبی: ساختار نانولولههای کربنی، شباهت بسیار زیادی به ساختار توبولها در رشتههای آکسونی دارد. به همین دلیل این نانولولهها یکی از داربستهای مناسب برای ترمیم بافت عصبی بهشمار میروند.
- بافت قلبی: هدایت الکتریکی نانولولههای کربنی، آنها را به یکی از گزینههای مناسب در مهندسی بافت قلب تبدیل میکند. کاشت نانولولههای کربنی در هیدروژلِ ژلاتین متاکریلات، داربستی دوبعدی بهوجود میآورد که شرایط رشد سلولهای ماهیچهای قلب را فراهم میکند. نانولولهها با بهبود اتصال سلول-سلول و انتقال جریان الکتریکی بین سلولی، شرایط ایجاد ضربان همزمان را در اختیار ماهیچه قلب قرار میدهد.
جمعبندی
مهندسی بافت تلاش میکند با ترکیب زیستشناسی، مهندسی مواد و مدلسازی، داربستها و بافتهای مصنوعی بسازد. هدف مهندسی بافت کمک به بازسازی یا جایگزینی بافت آسیبدیده است. ساختارهای مهندسی بافت از سه جز سلول، داربست و مولکولهای موردنیاز رشد سلول تشکیل میشود. دانشمندان تا به امروز نشان دادهاند که از این روش میتوان برای جایگزنی بخشی از بافت یا اندام کامل استفاده کرد و ممکن است این روش در آینده جایگزین پیوند عضو از انسان به انسان شود.

